78家醫療器械企業被國家通報,面臨停產威脅(附名單)
發布時間:2015/12/28 13:39:34
12月22日,CFDA公開了《國家醫療器械質量公告》(2015年第3期,總第8期),公告稱,國家食品藥品監督管理總局組織對一次性使用輸液器-帶針、B型超聲診斷設備(便攜式)、超聲彩色血流成像系統等65個品種990批(臺)的產品進行了質量監督抽驗和跟蹤抽驗。
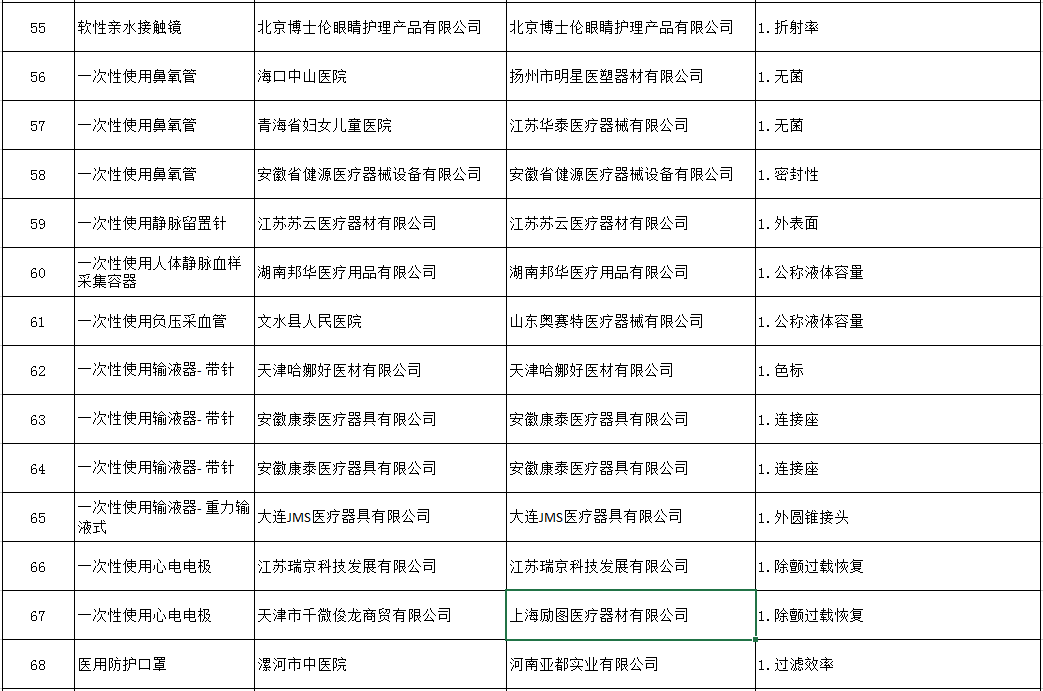
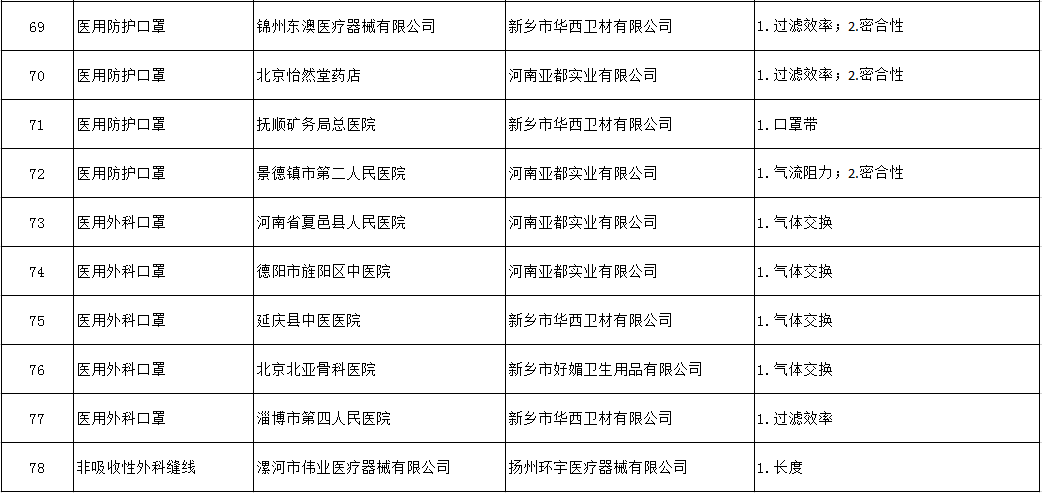
其中,有78個產品在抽驗中發現的不符合標準規定,企業所在地食品藥品監督管理部門已依據《醫療器械監督管理條例》(國務院令第650號)等有關規定進行了警告、責令停產停業、沒收產品及違法所得、行政罰款等行政處罰。
對不符合標準規定的產品,相關醫療器械生產企業應對不符合項目進行風險評估,根據醫療器械缺陷的嚴重程度確定召回級別,并由企業主動召回并公開召回信息(但至今我們還沒有看到本土企業有召回信息的發布)。企業所在地食品藥品監督管理部門應對企業召回情況進行監督,未組織召回的應責令召回;
如發現不符合標準規定醫療器械產品對人體造成傷害或者有證據證明可能危害人體健康的,食品藥品監督管理部門可以采取暫停生產、進口、經營、使用的緊急控制措施。相關省級食品藥品監督管理部門要督促企業查明原因、制定整改措施并限期整改,于2016年1月31日前將有關處置情況向社會公布。
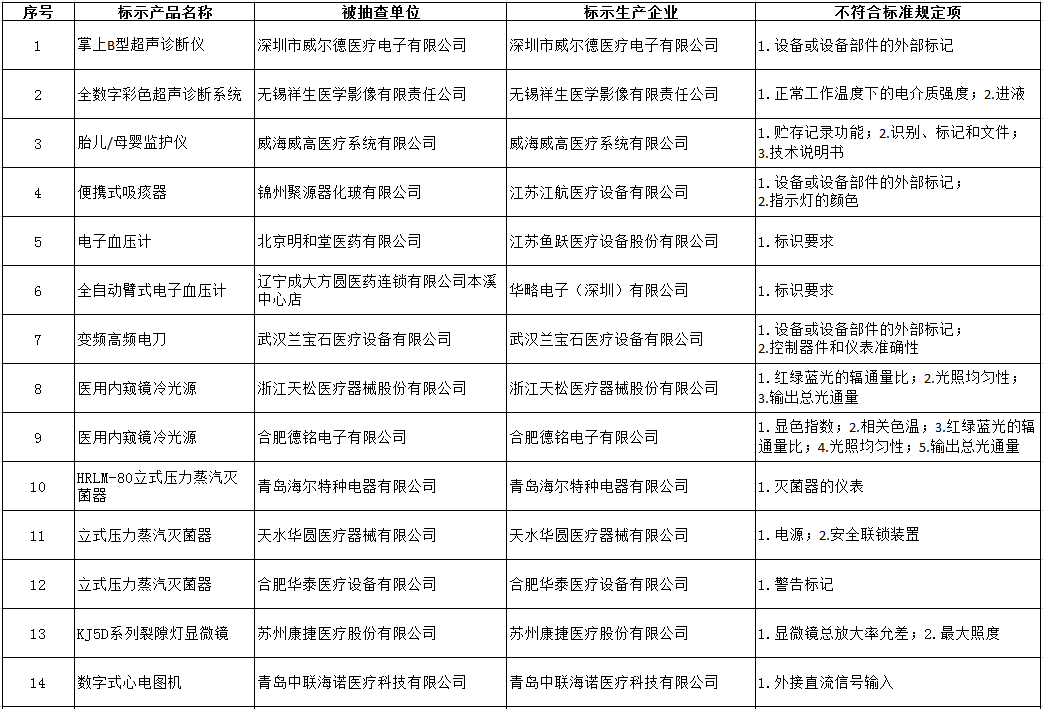
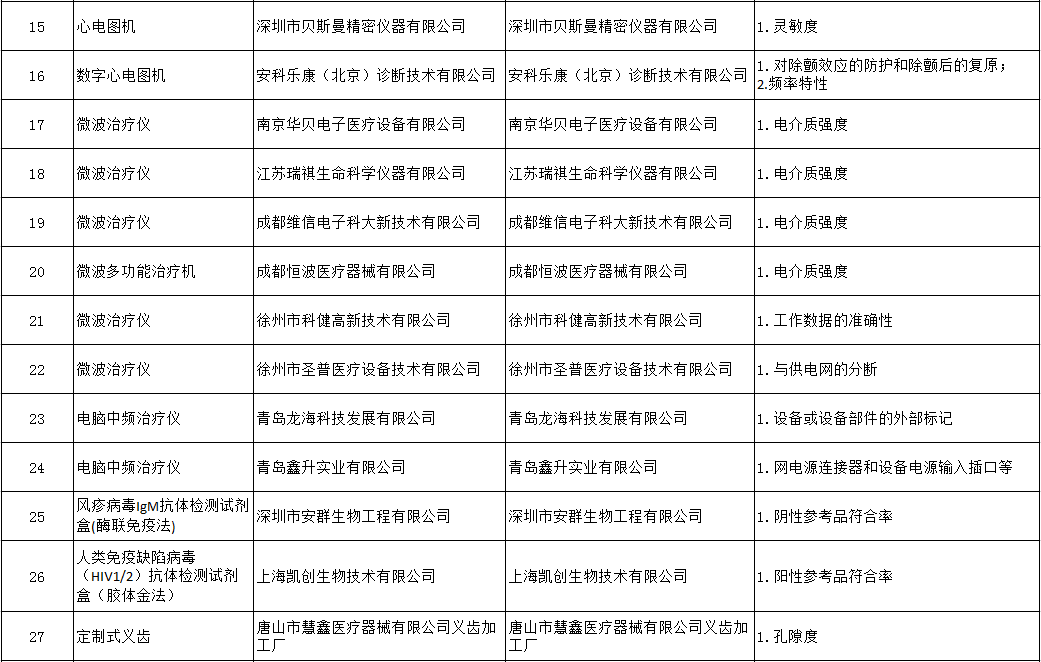
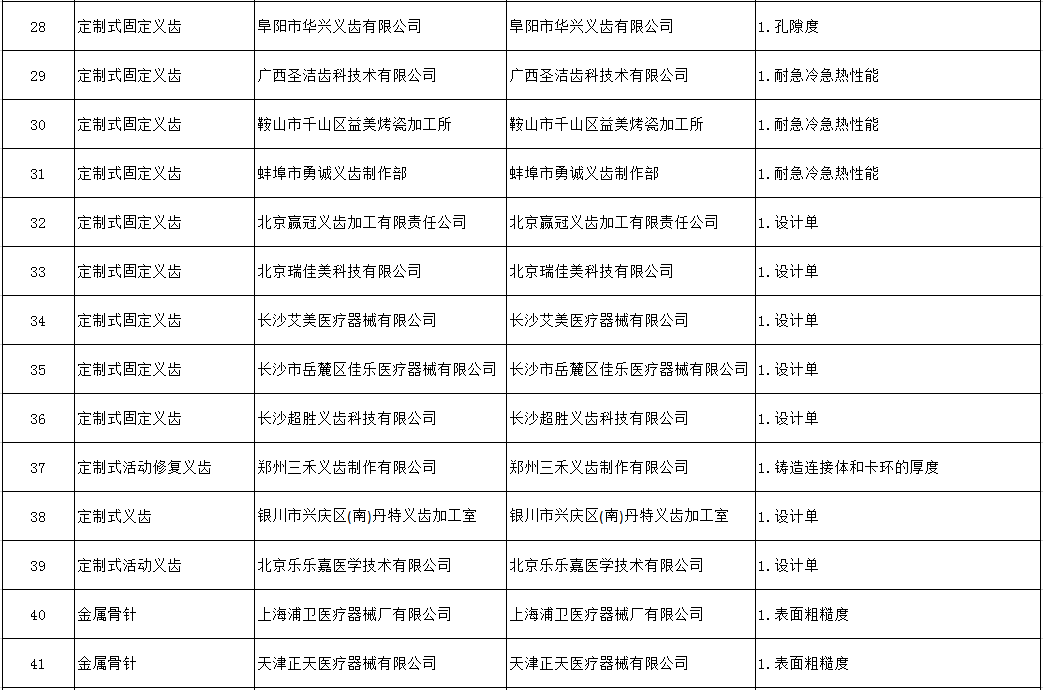
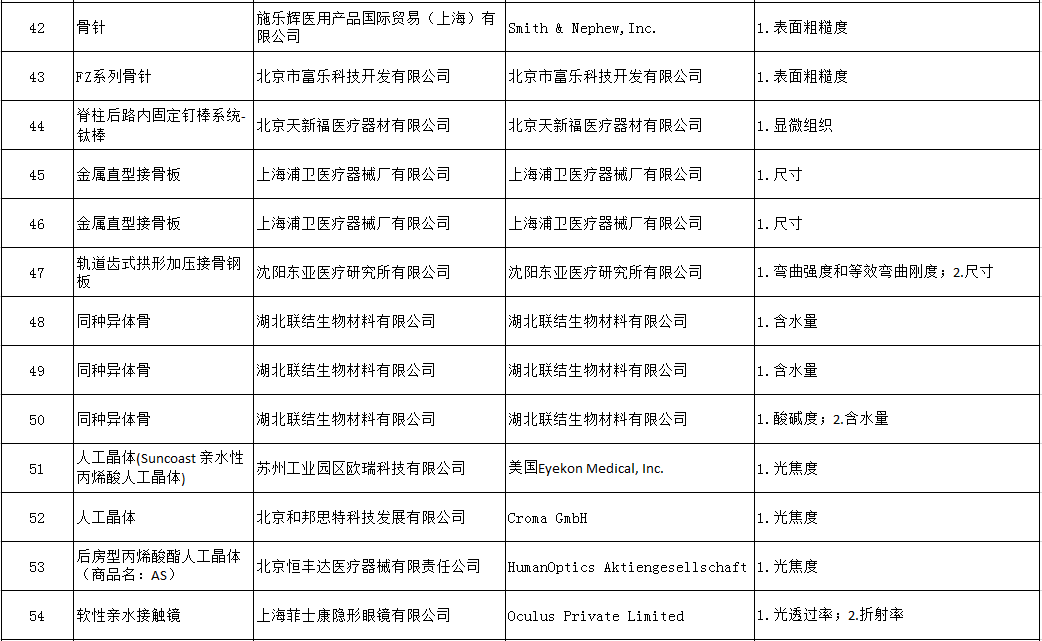
附:被罰企業名單