11省份77家企業新注冊186個醫療器械產品
國家食品藥品監督管理總局公布了今年前2個月批準注冊的醫療器械產品目錄,471個拿到批文的產品中,6成為進口,進口第三類器械有165個,進口二類120個。境內醫療器械產品只有歸屬第三類的186個。
由于名單實在太多,排布無序,進口那部分還用了英文、日文等,而且時間有限,中國醫療器械今天先為微友們送上境內產品的梳理情況。
按地域劃分,境內186個產品來自11省(直轄市)。江蘇最多49個,占到了超過四分之一。然后依次是北京38個,廣東18個,上海、天津各17個,浙江16個,福建14個,山東8個,四川6個,安徽2個,江西1個。
按企業劃分,186個產品來自77家企業。最多的是蘇州浩歐博生物醫藥有限公司,一家注冊了24個產品。博奧賽斯(天津)生物科技有限公司注冊了14個。
還有碧迪快速診斷產品(蘇州)有限公司和廈門萬泰凱瑞生物技術有限公司各自注冊了7個,北京潤諾思醫療科技有限公司和四川邁克生物各自注冊了6個,北京華大吉比愛生物技術有限公司和上海凱創生物技術有限公司各自注冊了5個。
按領域劃分,體外診斷產品占到了四分之三,又以試劑占據絕大多數。以上注冊數最多的都是IVD領域的。連國內械企龍頭深圳邁瑞都注冊了3個IVD產品。其他比較多的有一次性耗材、骨科假體、X射線機、各種治療儀。
從這2個月產品的注冊情況來看,還是比較能反映我國醫療器械行業現實的:集中在東部沿海發達地區,高端、高值、高性能的占比很少,IVD目前大受追捧。
此外,境內注冊產品也與進外注冊產品形成了鮮明對比,境外以設備和高值耗材居多,具體詳見中國醫療器械稍后分析。
以下為按地區、按企業重新整理后的186個產品名單:
江蘇省最多,涉及11家企業的49個產品

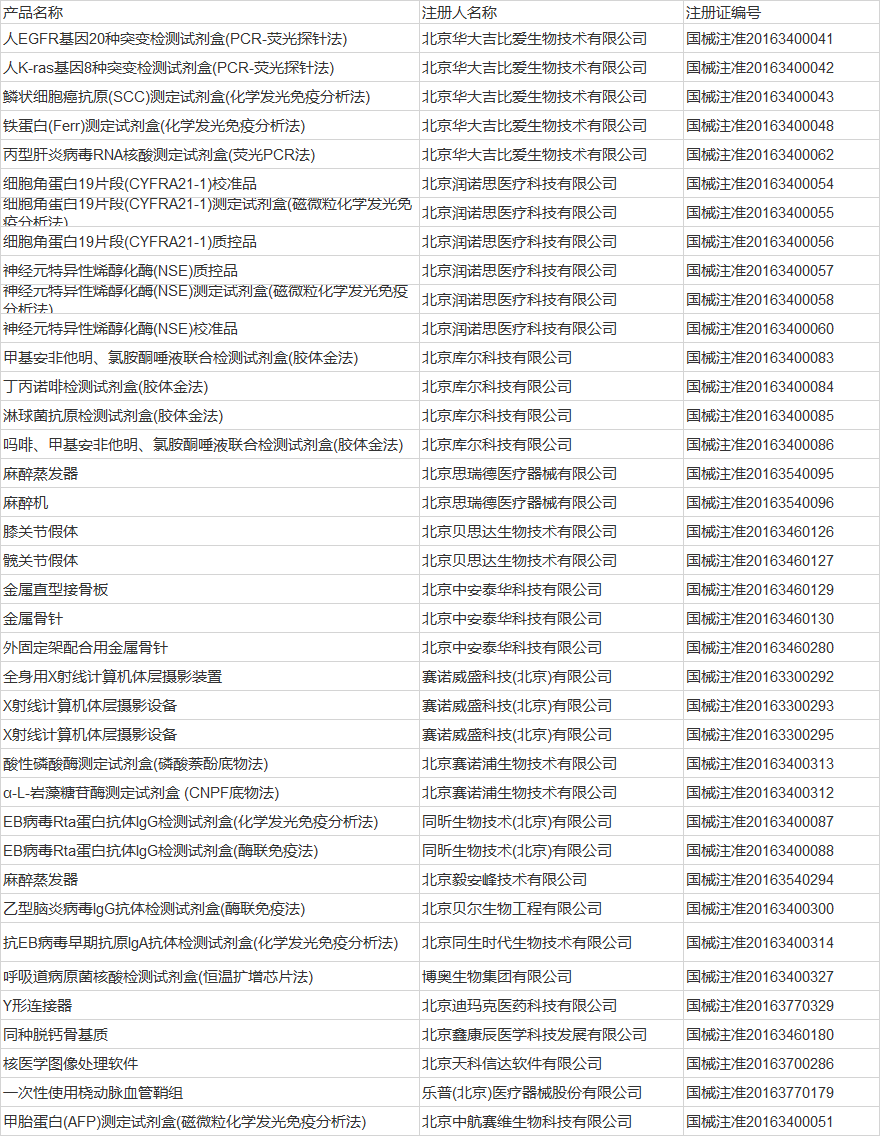
北京其次,涉及18家企業的38個產品
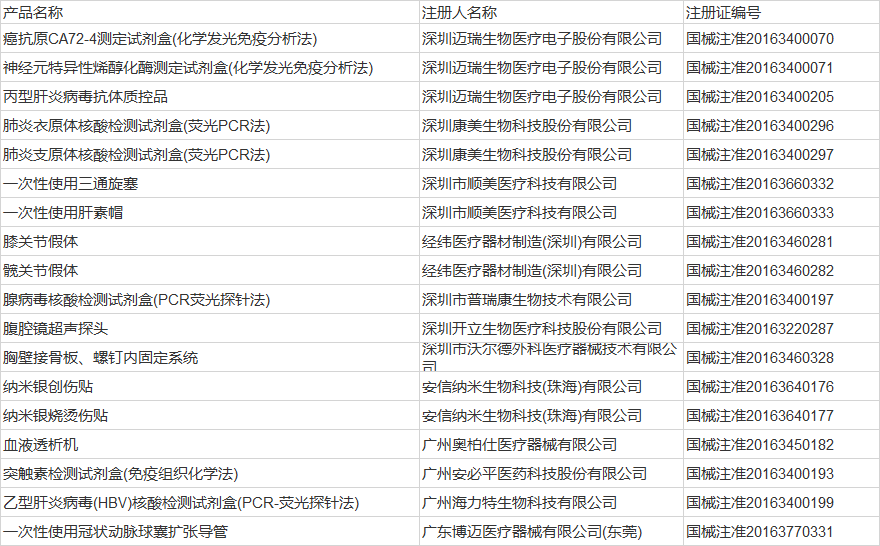
廣東12家企業的18個產品
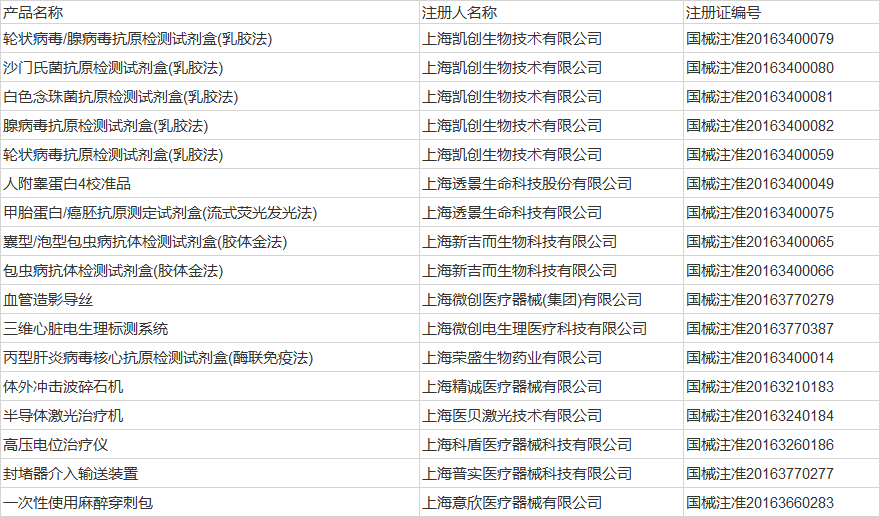
上海10家企業的17個產品
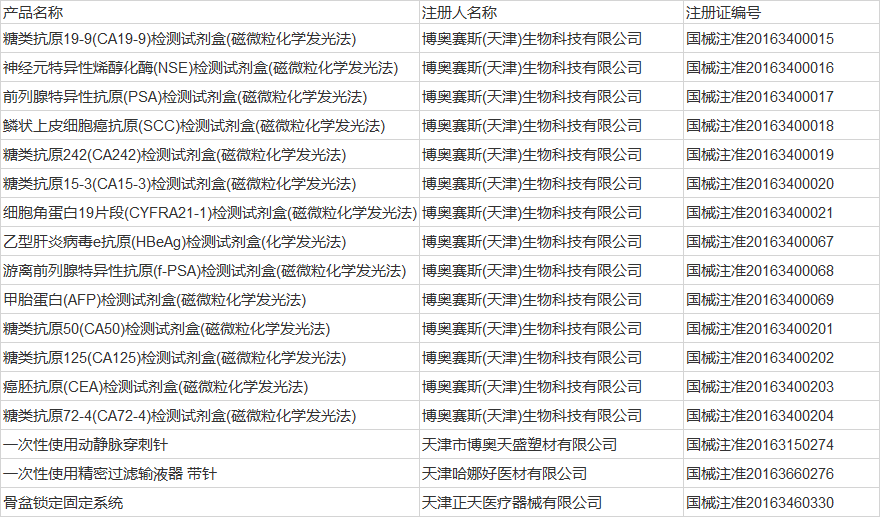
天津4家企業的17個產品
浙江11家企業的16個產品
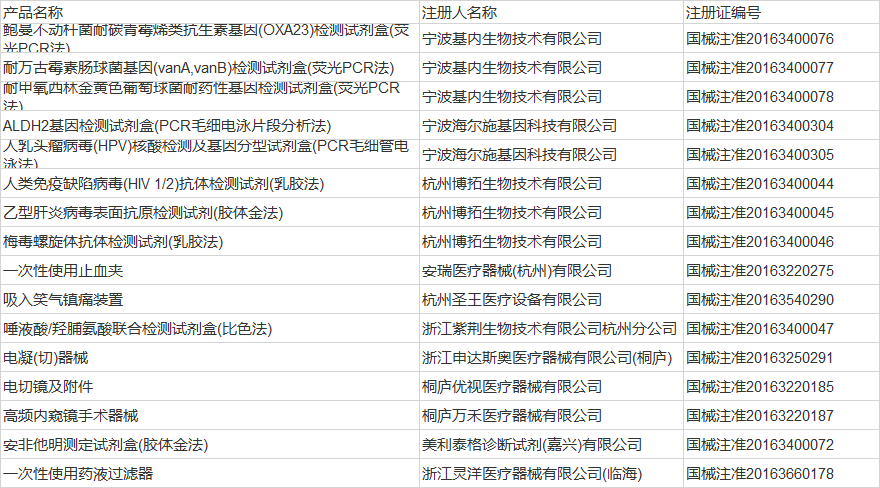
福建廈門4家企業的14個產品
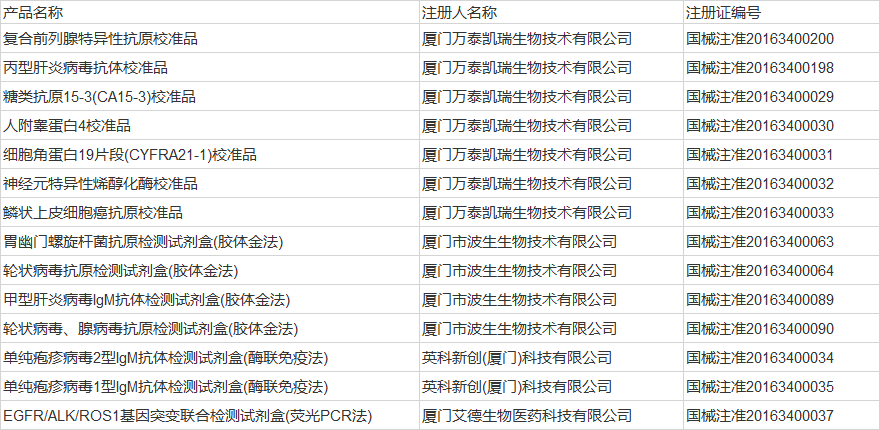
山東4家企業的8個產品
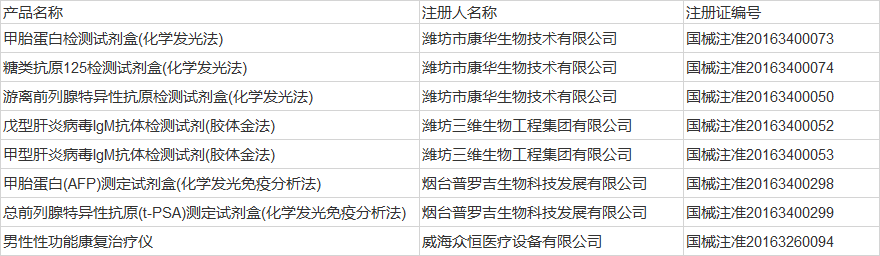
四川1家企業的6個產品
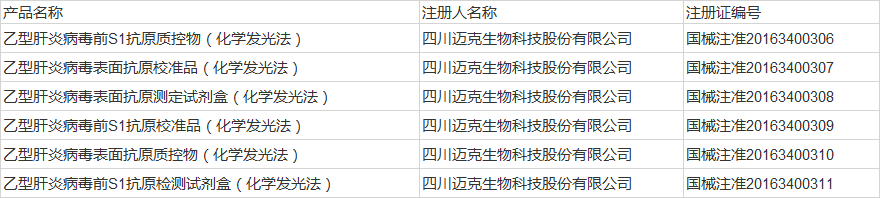
安徽1家企業的2個產品

江西1家企業的1個產品


相關閱讀
- 2022年底上海第二類醫療器械產品注冊周期縮短至6-7個月2021-05-21
- 這些耗材,多省不予上市!2021-03-10
- 上海自貿區“證照分離”有了升級版 醫療器械注冊證試行2017-12-18
- 新版醫療器械分類目錄實施在即2017-05-27
- 醫療器械召回管理辦法落地 徹底影響械企!2017-05-02






