二、三類醫療器械實名制,全國實行!
醫療器械“領證”大軍繼續擴員。全國范圍內,二類醫療器械唯一標識正式來襲。
01 103種器械,“實名制”管理
2月17日,國家藥監局、國家衛健委、國家醫保局發布《關于做好第三批實施醫療器械唯一標識工作的公告》,提出開展第三批醫療器械唯一標識工作。
截至目前,第三類醫療器械的唯一標識工作均已開展。全國范圍內,UDI也將進一步覆蓋部分二類醫療器械。
《公告》指出,按照風險程度和監管需要,確定部分臨床需求量較大的一次性使用產品、集中帶量采購中選產品、醫療美容相關產品等部分第二類醫療器械作為第三批醫療器械唯一標識實施品種。
共有103種醫療器械被納入此次唯一標識實施工作中,包括超聲手術設備、激光手術設備及附件、高頻/射頻手術設備及附件、內窺鏡手術用有源設備、神經和心血管手術器械-心血管介入器械、骨科手術器械、診斷X射線機、光治療設備、起搏系統分析設備、注射泵、臨床檢驗器械等。
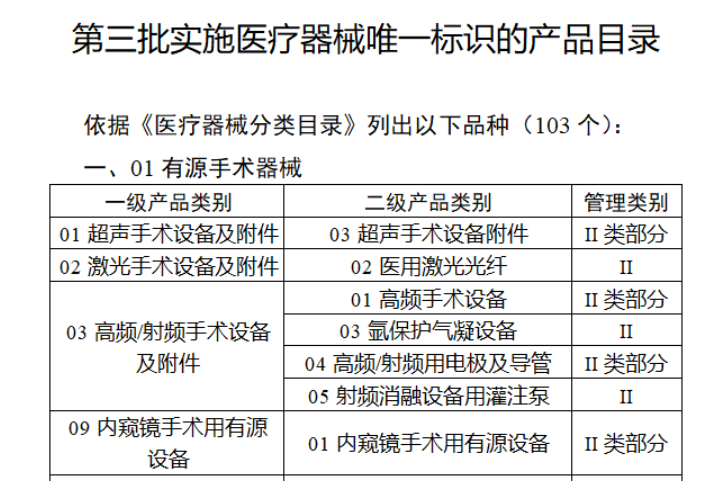
(完整清單附文末)
根據《公告》,對列入第三批實施產品目錄的醫療器械,注冊人應當按照時限要求有序開展以下工作:
2024年6月1日起生產的醫療器械應當具有醫療器械唯一標識;此前已生產的第三批實施唯一標識的產品可不具有唯一標識。生產日期以醫療器械標簽為準。
2024年6月1日起申請注冊的,注冊申請人應當在注冊管理系統中提交其產品最小銷售單元的產品標識;2024年6月1日前已受理或者獲準注冊的,注冊人應當在產品延續注冊或者變更注冊時,在注冊管理系統中提交其產品最小銷售單元的產品標識。
產品標識不屬于注冊審查事項,產品標識的單獨變化不屬于注冊變更范疇。
2024年6月1日起生產的醫療器械,在其上市銷售前,注冊人應當按照相關標準或者規范要求將最小銷售單元、更高級別包裝的產品標識和相關數據上傳至醫療器械唯一標識數據庫,確保數據真實、準確、完整、可追溯。
對于已在國家醫保局醫保醫用耗材分類與代碼數據庫中維護信息的醫療器械,要在唯一標識數據庫中補充完善醫保醫用耗材分類與代碼字段,同時在醫保醫用耗材分類與代碼數據庫維護中完善醫療器械唯一標識相關信息,并確認與醫療器械唯一標識數據庫數據的一致性。
當醫療器械最小銷售單元產品標識相關數據發生變化時,注冊人應當在產品上市銷售前,在醫療器械唯一標識數據庫中進行變更,實現數據更新。醫療器械最小銷售單元產品標識變化時,應當按照新增產品標識在醫療器械唯一標識數據庫上傳數據。
02 “身份證”捆綁:全周期可追溯
在醫療器械領域,以往流通使用環節無碼或者一物多碼現象普遍,給監管帶來阻力。
醫療器械唯一標識(Unique Device Identification,簡稱UDI)相當于是醫療器械的身份證,由產品標識和生產標識組成,產品標識是識別注冊人/備案人、醫療器械型號規格和包裝的唯一代碼;生產標識包括與生產過程相關的信息,包括產品批號、序列號、生產日期和失效日期等,可與產品標識聯合使用。
全球范圍內,UDI都是醫療器械監管領域關注的焦點和熱點。據了解,2013年,國際醫療器械監管機構論壇發布醫療器械唯一標識系統指南。同年,美國發布醫療器械唯一標識系統法規,要求利用7年時間全面實施醫療器械唯一標識。2017年,歐盟立法要求實施醫療器械唯一標識,日本、澳大利亞、阿根廷等國家也相繼開展相關工作。
國家醫保局此前指出,從政府管理角度,醫療器械監管部門利用UDI,可構建醫療器械監管大數據,實現醫療器械監管來源可查、去向可追、責任可究;衛生行政管理部門利用UDI,可提升對醫療用械使用行為的規范管理水平,推動建立健康醫療大數據;醫保部門利用UDI,有助于在招標采購中精準識別醫療器械,實現結算透明化,打擊欺詐行為。
而從產業發展角度,醫療器械注冊人備案人實施UDI,有助于提升企業信息化管理水平,建立產品追溯體系,提升企業管理效能;醫療器械經營企業實施UDI,可建立符合現代化的物流體系,實現醫療器械供應鏈的透明化、可視化、智能化;醫療機構實施UDI,可實現院內耗材精準管理,減少用械差錯。
2021年1月1日,國內9大類69種第三類醫療器械第一批實施醫療器械唯一標識。2022年6月1日,其他第三類醫療器械(含體外診斷試劑)第二批實施醫療器械唯一標識。
據賽柏藍器械觀察,此前已有海南、福建、四川、北京、天津等省市提前推進第二類醫療器械唯一標識工作,部分企業積極開展二類醫療器械UDI工作。
03多碼聯動,招采、支付透明化
伴隨國家層面UDI新規的出臺,接下來全國所有地區將全面推進前述醫療器械的唯一標識工作。
對于醫療器械注冊人而言,《公告》談到,要鼓勵基于唯一標識建立健全追溯體系,做好產品召回、追蹤追溯等有關工作。對于因《醫療器械分類目錄》動態調整導致產品管理類別發生變化的情況,醫療器械注冊人應當按照調整后管理類別的要求實施唯一標識。
《公告》還指出,醫療器械經營企業要在經營活動中積極應用唯一標識,做好帶碼入庫、出庫,實現產品在流通環節可追溯。
醫療機構要在臨床使用、支付收費、結算報銷等臨床實踐中積極應用唯一標識,做好全程帶碼記錄,實現產品在臨床環節可追溯。
值得關注的是,醫療器械身份證也將與國家醫保編碼關聯使用。
根據《公告》,省級藥品監督管理部門要加強唯一標識工作的培訓指導,結合實施工作推進需求做好產品注冊系統改造,組織轄區內醫療器械注冊人按要求開展產品賦碼、數據上傳和維護工作,加強與轄區內衛生、醫保部門協同,推動三醫聯動。
省級衛生健康部門要指導轄區內醫療機構積極應用唯一標識,加強醫療器械在臨床應用中的規范管理。
省級醫保部門要加強醫保醫用耗材分類與代碼與醫療器械唯一標識的關聯使用,推動目錄準入、支付管理、帶量招標等的透明化、智能化。
目前,國家醫保編碼的推進工作已進入最后一公里。兩碼聯動后,醫療器械全鏈條也將迎來全新監管。
附件:
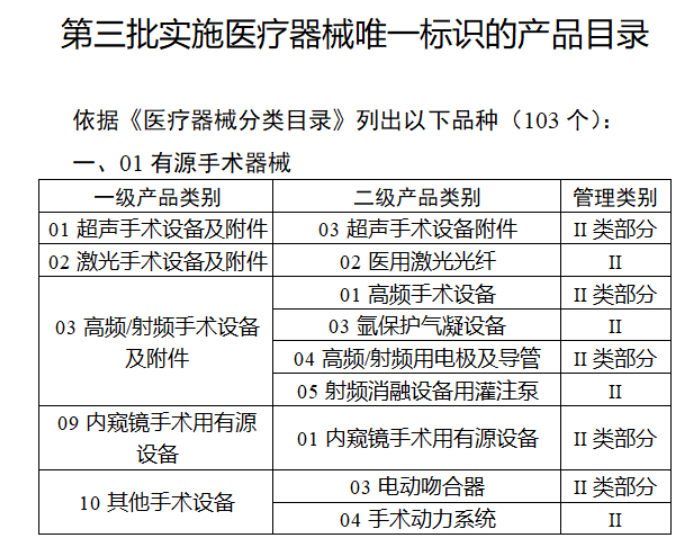
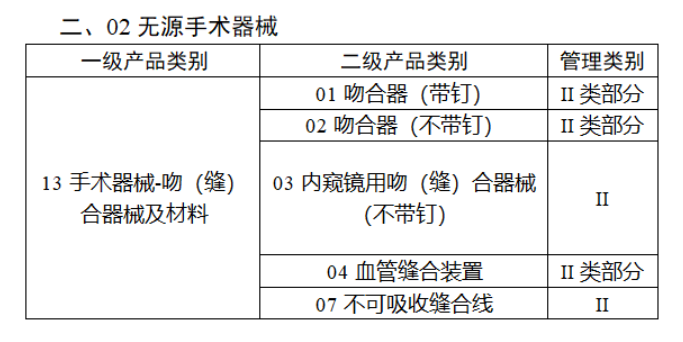
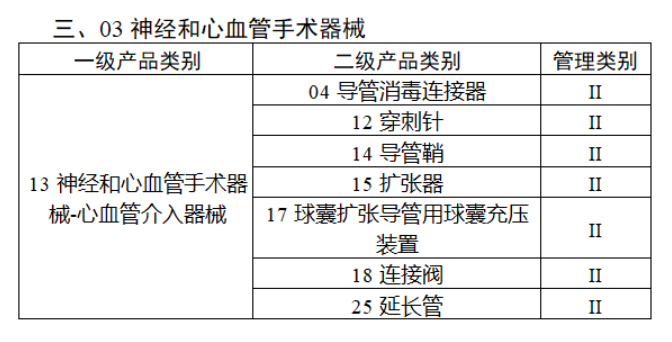
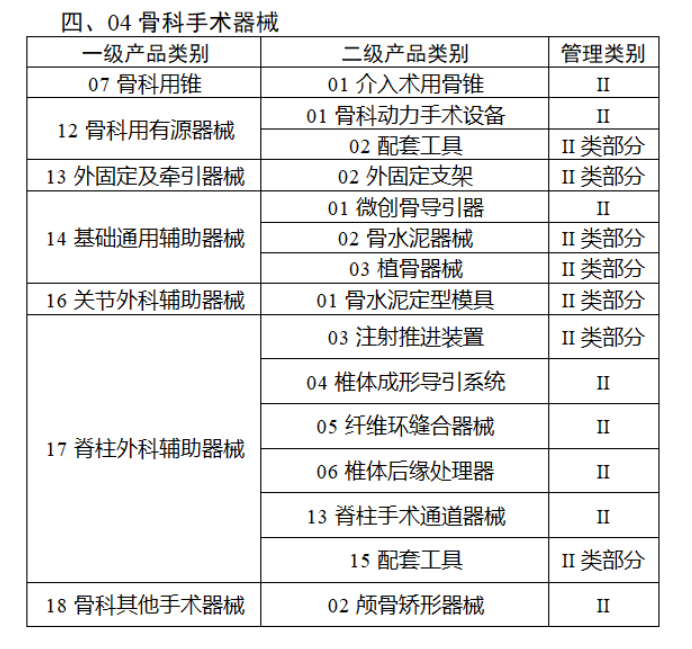
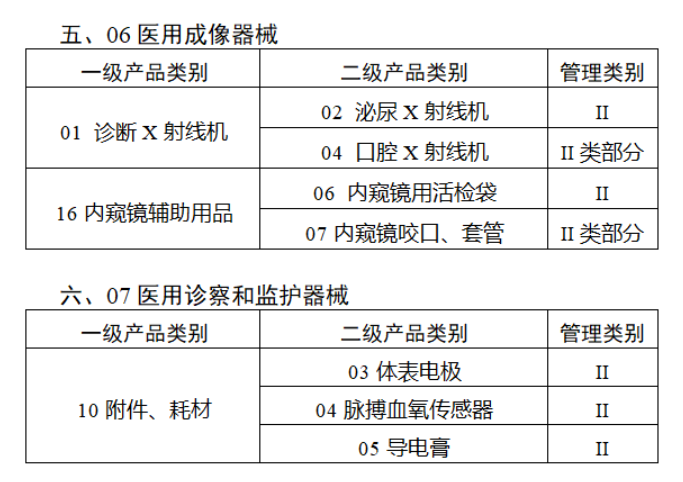
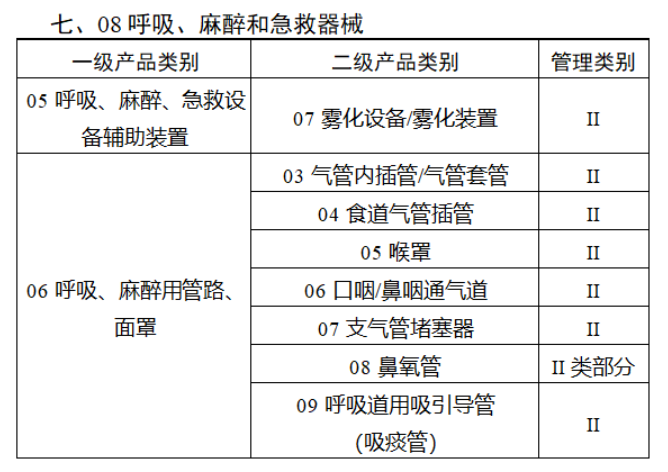
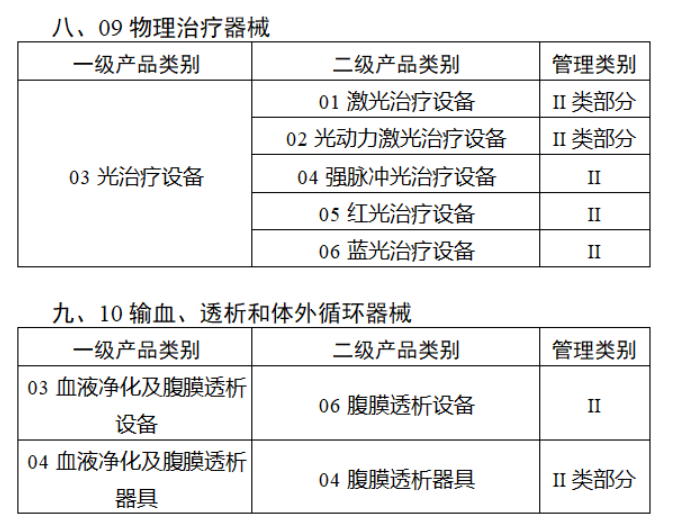
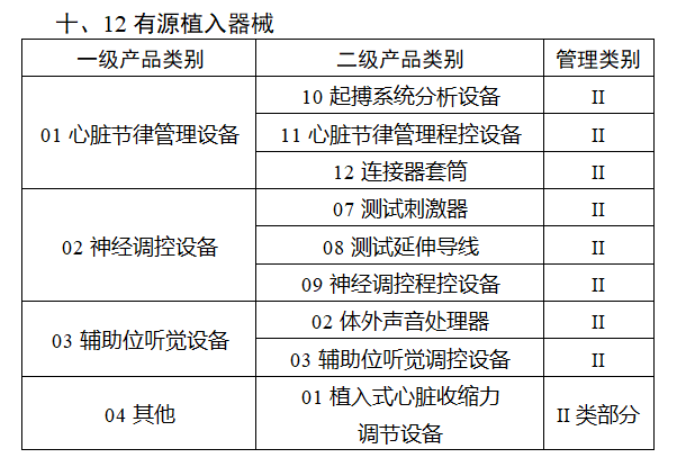
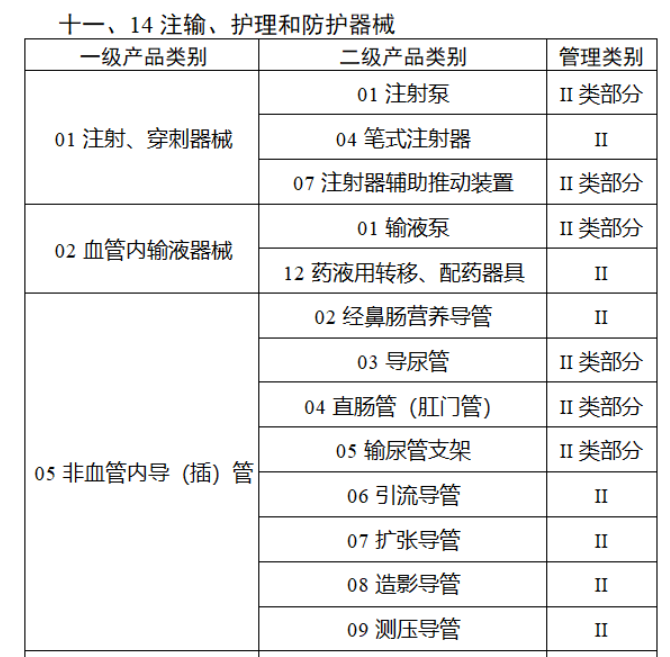
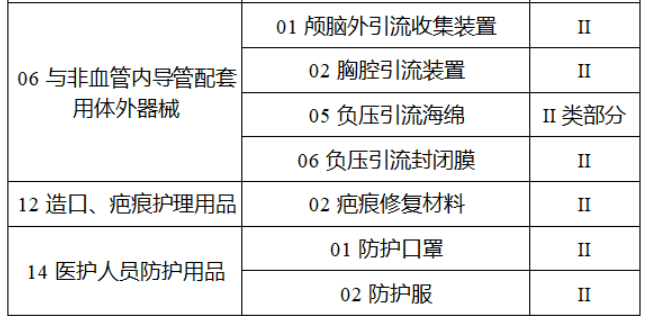
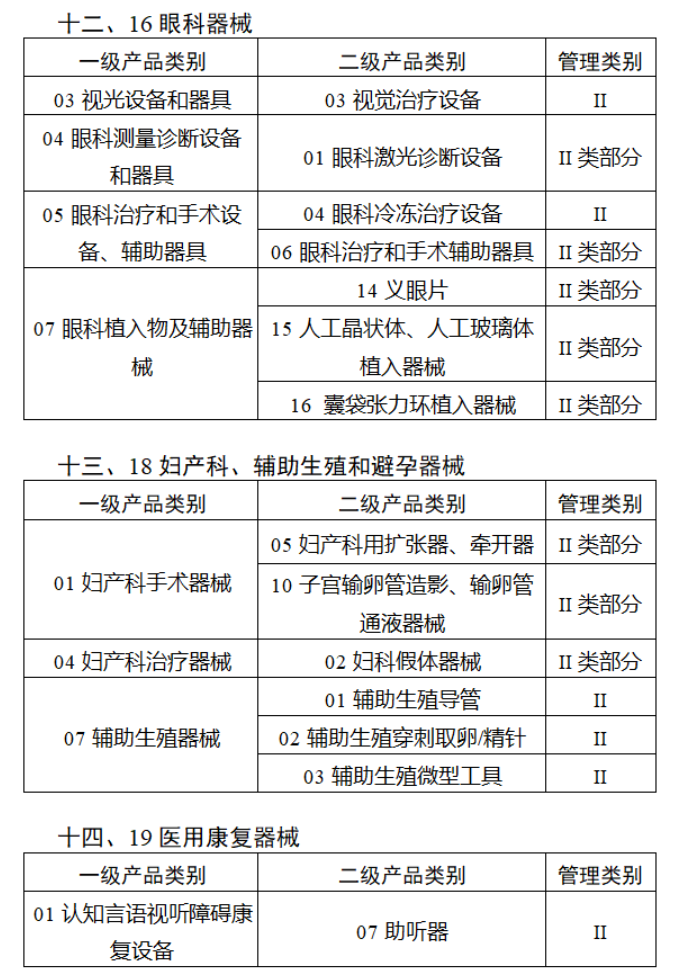
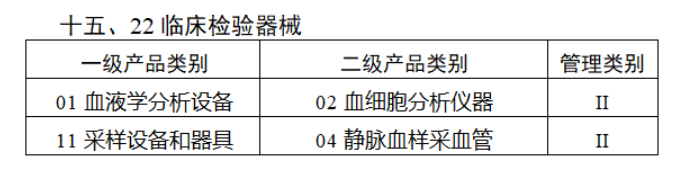
【來源:賽柏藍器械】

下一篇:紀委通報:耗材回款難,整改!
相關閱讀
- 官方發文,一、二類醫療器械「實名制」2023-04-20
- 三部門發文,醫療器械「實名制」擴圍!2023-04-06
- 6月1日起,第三類醫療器械全面覆蓋唯一標識2022-05-19
- 正式文件:69類醫療器械開始編碼(附目錄)2021-04-23






